Ο Άγγλος επιστήμονας Τζων Ντάλτον (John Dalton) πέθανε σαν σήμερα το 1844
 |
| Άγαλμα του Dalton από τον Chantrey |
Ο Dalton ανακάλυψε ότι η πίεση των κορεσμένων ατμών ενός υγρού στο σημείο βρασμού έχει την ίδια τιμή για όλα τα υγρά και θεμελίωσε το νόμο των μερικών πιέσεων του Dalton.
Δημοσίευσε για ποικίλα θέματα όπως η βροχή η δροσιά και η προέλευση των πηγών (υδρόσφαιρα), για τη θερμότητα, το χρώμα του ουρανού, τον ατμό και την ανάκλαση και διάθλαση του φωτός. Αλλά και για την γραμματική όπως για τα βοηθητικά ρήματα και τις μετοχές της αγγλικής γλώσσας.
Τα πέντε κύρια σημεία της ατομικής θεωρίας του Ντάλτον
- Τα στοιχεία αποτελούνται από εξαιρετικά μικρά σωματίδια που ονομάζονται άτομα.
- Τα άτομα ενός συγκεκριμένου στοιχείου είναι ίδια σε μέγεθος, μάζα, και άλλες ιδιότητες. Τα άτομα διαφορετικών στοιχείων διαφέρουν σε μέγεθος, μάζα, και άλλες ιδιότητες.
- Τα άτομα δεν μπορούν να υποδιαιρεθούν, να δημιουργηθούν ή να καταστραφούν.
- Άτομα διαφορετικών στοιχείων συνδυάζονται σε απλές ακέραιες αναλογίες για να σχηματίσουν χημικές ενώσεις.
- Στις χημικές αντιδράσεις, τα άτομα συνδυάζονται, διαχωρίζονται, ή αναδιατάσσονται.
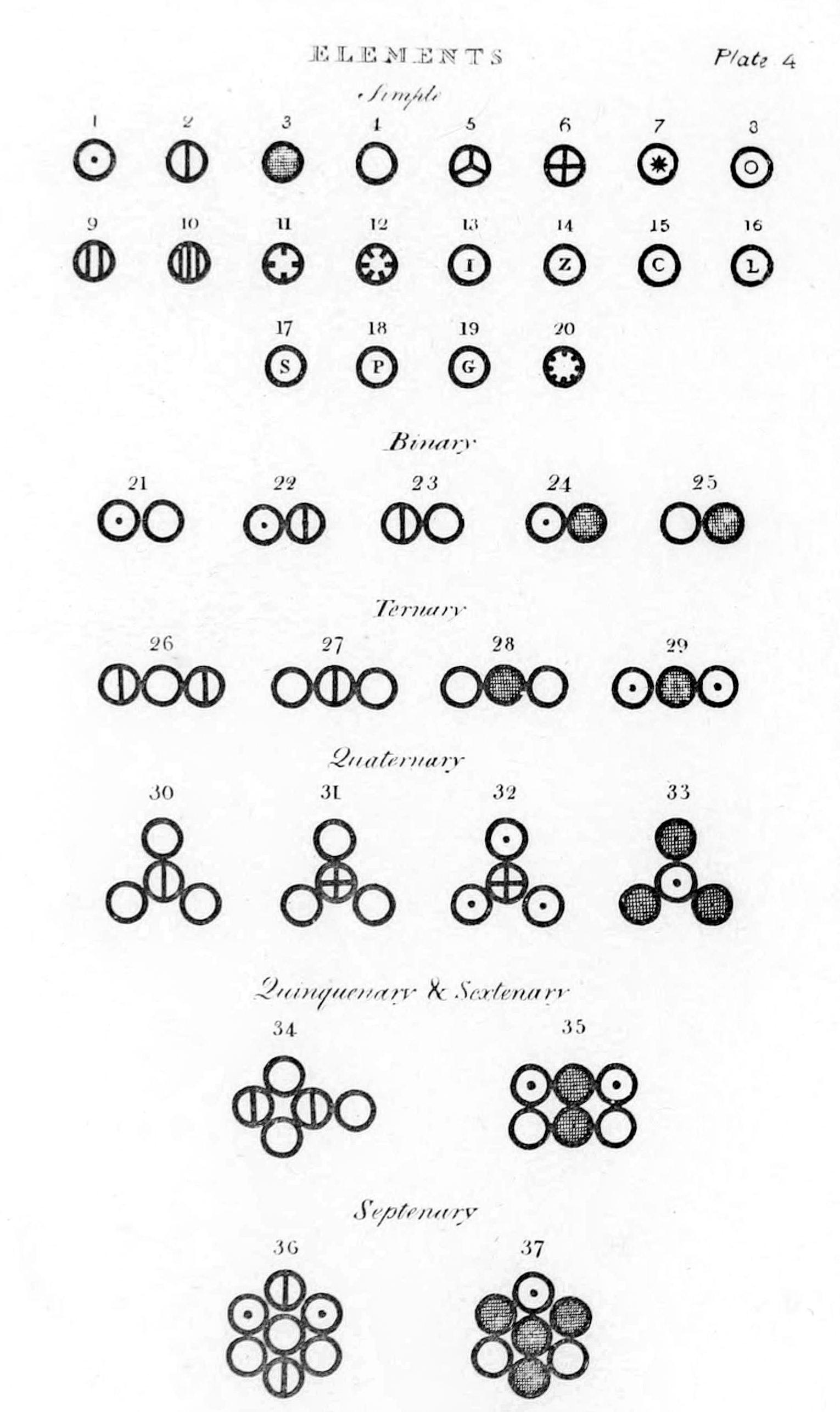
Όταν τα άτομα συνδυάζονται σε μια μόνο αναλογία, «.. θα πρέπει να θεωρείται ότι είναι δυαδική, εκτός αν κάποιο αίτιο οδηγεί στο αντίθετο συμπέρασμα».Αυτό ήταν απλώς μια υπόθεση προερχόμενη από την πίστη στην απλότητα της φύσης. Δεν υπήρχαν τότε διαθέσιμα αποδεικτικά στοιχεία ώστε οι επιστήμονες να συμπεράνουν πόσα άτομα από κάθε στοιχείο συνδυάζονται για να σχηματίσουν σύνθετα μόρια. Αλλά αυτός ή κάποιος άλλος τέτοιος κανόνας ήταν απολύτως απαραίτητος σε κάθε αρχική θεωρία, δεδομένου ότι χρειάζεται ένας υποτιθέμενος μοριακός τύπος, προκειμένου να υπολογιστούν τα σχετικά ατομικά βάρη. Σε κάθε περίπτωση, ο «κανόνας της μέγιστης απλότητας» του Ντάλτον τον ανάγκασε να υποθέσει ότι ο τύπος για το νερό ήταν ΟΗ και αμμωνίας ήταν NH, αρκετά διαφορετικά από τις σύγχρονες αντιλήψεις μας.
Παρά τις αβεβαιότητες για την ατομική θεωρία του Ντάλτον, οι αρχές της επέζησαν. Η πεποίθηση πως τα άτομα δεν μπορούν να διαιρεθούν, να δημιουργηθούν ή να καταστραφούν σε μικρότερα σωματίδια όταν συνδυαστούν, διαχωριστούν ή ανακαταταχθούν κατά τη διάρκεια χημικών αντιδράσεων, έρχεται σε αντίθεση με την ύπαρξη της πυρηνικής σχάσης και της πυρηνικής σύντηξης, όμως αυτές οι διαδικασίες είναι πυρηνικές αντιδράσεις και όχι χημικές. Επιπρόσθετα, η ιδέα πως όλα τα άτομα ενός στοιχείου είναι ίδια ως προς τις φυσικές και χημικές τους ιδιότητες δεν είναι ακριβής, διότι πλέον γνωρίζουμε πως τα ισότοπα των στοιχείων έχουν ελαφρώς διαφορετικά βάρη. Ωστόσο, ο Ντάλτον είχε διατυπώσει μια πολύ ισχυρή και σημαντική θεωρία. Πράγματι, η καινοτόμος θεωρία του Ντάλτον αποδείχτηκε εξίσου σημαντική για το μέλλον της επιστήμης όπως υπήρξε και αυτή του Αντουάν Λαβουαζιέ σχετικά με την βασισμένη στο οξυγόνο χημεία.
Από τη: Royal Society of Chemistry (RSC) και από τη Βικιπαίδεια, την ελεύθερη εγκυκλοπαίδεια: Τζων Ντάλτον
Εικόνα: By No machine-readable author provided. Kaihsu assumed (based on copyright claims). - No machine-readable source provided. Own work assumed (based on copyright claims)., CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=383000
By haade - En.wiki, Public Domain, https://commons.wikimedia.org/w/index.php?curid=1387026
Εικόνα: By No machine-readable author provided. Kaihsu assumed (based on copyright claims). - No machine-readable source provided. Own work assumed (based on copyright claims)., CC BY-SA 3.0, https://commons.wikimedia.org/w/index.php?curid=383000
By haade - En.wiki, Public Domain, https://commons.wikimedia.org/w/index.php?curid=1387026